
血管內(nèi)皮細(xì)胞不僅在機體組織的氧氣和營養(yǎng)供給方面發(fā)揮著重要作用,還與血管內(nèi)皮生長因子共同驅(qū)動了新血管的生成,在腫瘤等疾病的血管新生中發(fā)揮重要作用。抗腫瘤血管新生(anti-angiogenesis)治療是以血管內(nèi)皮細(xì)胞為靶點,通過抑制內(nèi)皮細(xì)胞增殖和遷移、改變腫瘤生長微環(huán)境,從而抑制腫瘤生長過程中的血管新生,切斷腫瘤的供養(yǎng),最終達(dá)到遏制腫瘤生長和轉(zhuǎn)移的目的。深入解析血管新生分子機制,探尋潛在關(guān)鍵治療靶點對于腫瘤治療至關(guān)重要。
腫瘤團(tuán)隊多年來研究證實G蛋白抑制性α亞單位1和3(Gαi1/3蛋白)是腫瘤進(jìn)程中的關(guān)鍵靶點。在多個細(xì)胞和生長因子刺激下,Gαi1/3和受體酪氨酸激酶(RTKs)等受體結(jié)合介導(dǎo)下游信號轉(zhuǎn)導(dǎo)(Protein & Cell 2022 [1], Oncogene 2018, 2021[2, 3],IJBS 2022[4],Theranostics 2018,2021a/b[5-7]等論文)。Science雜志的Senior Editor Dr. Brian Ray評述:“Gαi蛋白可能是抑制癌細(xì)胞的治療靶點”。
磷酸烯醇丙酮酸羧激酶1(PCK1)是催化糖異生關(guān)鍵限速酶。2021年腫瘤團(tuán)隊在Nature子期刊Cell Death & Disease雜志(IF:8.469)發(fā)表了“Identification of phosphoenolpyruvate carboxykinase 1 as a potential therapeutic target for pancreatic cancer(PCK1作為胰腺癌潛在治療靶點的鑒定)”的研究論文[8],發(fā)現(xiàn)PCK1作為激酶在胰腺癌中高表達(dá)并發(fā)揮著重要的生物學(xué)作用,并且可能可以成為潛在的胰腺癌治療靶點。2022年5月27日,腫瘤團(tuán)隊在Science Advances(Science 子刊,IF=14.143)發(fā)表了題為“The requirement of phosphoenolpyruvatecarboxykinase 1 for angiogenesis in vitro and in vivo”研究論文,該研究揭示了PCK1在促Gαi3表達(dá)及血管新生中的關(guān)鍵作用。

研究發(fā)現(xiàn)在體外培養(yǎng)的人臍靜脈內(nèi)皮細(xì)胞、人視網(wǎng)膜毛細(xì)血管內(nèi)皮細(xì)胞和人腦微血管內(nèi)皮細(xì)胞中,敲減及敲除PCK1抑制細(xì)胞成管、增殖、遷移、浸潤及出芽;而過表達(dá)PCK1促體外血管新生作用。C57小鼠內(nèi)皮細(xì)胞特異性敲減PCK1后顯著抑制P1(出生后第一天)到P5小鼠視網(wǎng)膜血管發(fā)育;在成年小鼠中,PCK1敲減導(dǎo)致視網(wǎng)膜血管滲漏和無細(xì)胞毛細(xì)血管生長,同時降低視網(wǎng)膜神經(jīng)節(jié)細(xì)胞的數(shù)量。
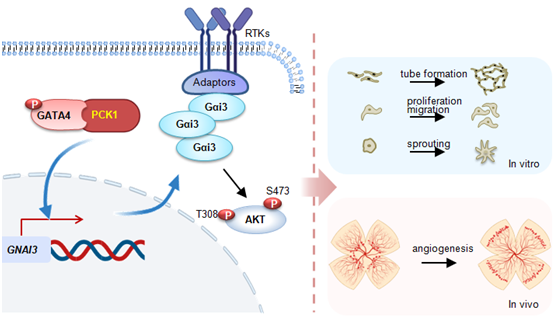
機制研究發(fā)現(xiàn)PCK1的促血管作用并不依賴于其促糖異生功能。PCK1與轉(zhuǎn)錄因子GATA4互作并促GATA4磷酸化;后者通過與Gαi3啟動子結(jié)合,促Gαi3轉(zhuǎn)錄、表達(dá)及下游Akt的活化,最終導(dǎo)致血管新生。而敲減、敲除PCK1幾乎阻斷GATA4磷酸化,下調(diào)Gαi3表達(dá)及Akt的活化。總之,PCK1通過介導(dǎo)Gαi3表達(dá)及Akt活化促血管新生。PCK1是血管新生的新靶點。
原文鏈接:http://doi.org/10.1126/sciadv.abl9806
腫瘤團(tuán)隊陳敏斌教授和曹聰教授是該論文的共同通訊作者。
參考文獻(xiàn)
1. Liu F, Chen G, Zhou L, Wang Y, Zhang Z, Qin X, Cao C. YME1L overexpression exerts pro-tumorigenic activity in glioma by promoting Gαi1 expression and Akt activation. Protein Cell. 2022.
2. Liu YY, Chen MB, Cheng L, Zhang ZQ, Yu ZQ, Jiang Q, Chen G, Cao C. microRNA-200a downregulation in human glioma leads to Galphai1 over-expression, Akt activation, and cell proliferation. Oncogene. 2018; 37: 2890-902.
3. Lv Y, Wang Y, Song Y, Wang SS, Cheng KW, Zhang ZQ, Yao J, Zhou LN, Ling ZY, Cao C. LncRNA PINK1-AS promotes G alpha i1-driven gastric cancer tumorigenesis by sponging microRNA-200a. Oncogene. 2021; 40: 3826-44.
4. Bian ZJ, Shan HJ, Zhu YR, Shi C, Chen MB, Huang YM, Wang XD, Zhou XZ, Cao C. Identification of Galphai3 as a promising target for osteosarcoma treatment. Int J Biol Sci. 2022; 18: 1508-20.
5. Wang Y, Liu YY, Chen MB, Cheng KW, Qi LN, Zhang ZQ, Peng Y, Li KR, Liu F, Chen G, Cao C. Neuronal-driven glioma growth requires Galphai1 and Galphai3. Theranostics. 2021; 11: 8535-49.
6. Bai JY, Li Y, Xue GH, Li KR, Zheng YF, Zhang ZQ, Jiang Q, Liu YY, Zhou XZ, Cao C. Requirement of Galphai1 and Galphai3 in interleukin-4-induced signaling, macrophage M2 polarization and allergic asthma response. Theranostics. 2021; 11: 4894-909.
7. Sun J, Huang W, Yang SF, Zhang XP, Yu Q, Zhang ZQ, Yao J, Li KR, Jiang Q, Cao C. Galphai1 and Galphai3mediate VEGF-induced VEGFR2 endocytosis, signaling and angiogenesis. Theranostics. 2018; 8: 4695-709.
8. Zhu XR, Peng SQ, Wang L, Chen XY, Feng CX, Liu YY, Chen MB. Identification of phosphoenolpyruvate carboxykinase 1 as a potential therapeutic target for pancreatic cancer. Cell Death Dis. 2021; 12: 918.
服務(wù)熱線: 0512-57559009
母嬰熱線: 0512-57026117
東部新院區(qū):昆山市前進(jìn)東路566號

關(guān)注微信公眾號
Copyright ? 2013 昆山市第一人民醫(yī)院 版權(quán)所有 未經(jīng)許可不得轉(zhuǎn)載 蘇ICP備14019617號